Einfache Kohlenwasserstoffe: Unterschied zwischen den Versionen
DiMedS (Diskussion | Beiträge) |
DiMedS (Diskussion | Beiträge) |
||
| Zeile 11: | Zeile 11: | ||
===Alkane=== | ===Alkane=== | ||
Die Alkane zählen in der [[Organische Chemie|Organischen Chemie]] zu den einfachsten Kohlenwasserstoffe. Sie sind kettenförmig und in den Molekülen nur über Einfachbindungen verbunden. Als einfachstes Alkan zählt das [[Methan]] (CH<sub>4</sub>). Dieses besteht aus einem Kohlenstoffatom, welches je ein Elektronenpaar mit vier Wasserstoffatomen ausbildet. Diese vier bindenden Elektronenpaare stoßen sich gegenseitig ab und nehmen den größtmöglichen Abstand zueinander ein, weshalb die vier Wasserstoffatome ein Tetraeder bilden, in dessen Zentrum sich das Kohlenstoffatom befindet. Methan zählt als Hauptbestandteil des Erdgases und zählt als ein starkes Treibhausgas, welches einen viermal höheren Treibhauseffekt aufweist als Kohlenstoffdioxid. <br/> | Die Alkane zählen in der [[Organische Chemie|Organischen Chemie]] zu den einfachsten Kohlenwasserstoffe. Sie sind kettenförmig und in den Molekülen nur über Einfachbindungen verbunden. Als einfachstes Alkan zählt das [[Methan]] (CH<sub>4</sub>). Dieses besteht aus einem Kohlenstoffatom, welches je ein Elektronenpaar mit vier Wasserstoffatomen ausbildet. Diese vier bindenden Elektronenpaare stoßen sich gegenseitig ab und nehmen den größtmöglichen Abstand zueinander ein, weshalb die vier Wasserstoffatome ein Tetraeder bilden, in dessen Zentrum sich das Kohlenstoffatom befindet. Methan zählt als Hauptbestandteil des Erdgases und zählt als ein starkes Treibhausgas, welches einen viermal höheren Treibhauseffekt aufweist als Kohlenstoffdioxid. <br/> | ||
{|class="wikitable" style="margin:auto" | {|class="wikitable" style="float:right; margin:auto" | ||
|+homologe Reihe der Alkane | |+homologe Reihe der Alkane | ||
|- | |- | ||
| Zeile 38: | Zeile 37: | ||
|Decan||CH<sub>3</sub>-(CH<sub>2</sub>)<sub>8</sub>-CH<sub>3</sub>||C<sub>10</sub>H<sub>22</sub> | |Decan||CH<sub>3</sub>-(CH<sub>2</sub>)<sub>8</sub>-CH<sub>3</sub>||C<sub>10</sub>H<sub>22</sub> | ||
|} | |} | ||
Es sind zahlreiche Kohlenwasserstoffe mit einer Methan ähnlichen Struktur bekannt, welche in der '''homologen Reihe der Alkane''' zusammengefasst werden. Hierbei beschreibt der Wortstamm die Anzahl der Kohlenstoffatome in einem Alkanmolekül. Die Namen der Alkane werden aus diesen Wortstämmen und der '''Endung ''-an'' ''' gebildet. | |||
Die Alkane unterscheiden sich immer um eine Kohlenstoffatom und zwei Wasserstoffatome, also um eine -CH<sub>2</sub>-Gruppe. Daraus lässt sich die allgemeine Summenformel für die Alkane ableiten: '''C<sub>n</sub>H<sub>2n+2</sub> | |||
Aufgrund der immer gleichen Sturktur der Alkane zeigen sie ähnliche [[chemische Eigenschaften|chemische]] und [[physikalische Eigenschaften]]. Ein Beispiel hierfür ist die Verbrennung: Alkane verbrennen bei ausreichender Sauerstoffzufuhr immer vollständig unter Wärmeabgabe zu [[Kohlenstoffdioxid]] und [[Wasser]]. | |||
Version vom 24. August 2022, 12:54 Uhr
Einfache Kohlenwasserstoffe
Einfache Kohlenwasserstoffe sind organische Verbindungen, welche aus den Elementen Kohlenstoff C und Wasserstoff H bestehen. Zu diesen zählen die Alkane, Alkene und Alkine, wobei Alkane als gesättigte Kohlenwasserstoffe gelten und die Alkene und Alkine zu den ungesättigten Kohlenwasserstoffen zählen. Die einfachen Kohlenwasserstoffe werden zu den Aliphatischen Kohlenwasserstoffen gezählt, da es sich hierbei um kettenförmige, verzweigte oder unverzweigte Kohlenwasserstoffe handelt.
Einteilung ausgewählter Kohlenwasserstoff-Gruppen
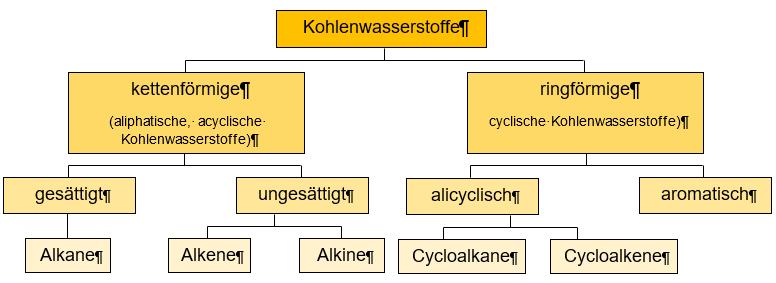
Kohlenwasserstoffe können in zwei Hauptgruppen eingeteilt werden: Die kettenförmigen (Aliphatische Kohlenwasserstoffe und Acyclische Kohlenwasserstoffe) und die ringförmigen (cyclische Kohlenwasserstoffe) Kohlenwasserstoffe. Kettenförmige Kohlenwasserstoffe können nun weiter unterteilt werden in die gesättigten (Alkane) und ungesättigten (Alkene und Alkine) Kohlenwasserstoffe und die ringförmigen Kohlenwasserstoffe in die alicyclischen (Cycloalkane und Cycloalkene) und aromatischen Kohlenwasserstoffe.
In diesem Beitrag sollen die einfachen, also Kettenförmigen Kohlenwasserstoffe, betrachtet werden.
kettenförmige Kohlenwasserstoffe
Alkane
Die Alkane zählen in der Organischen Chemie zu den einfachsten Kohlenwasserstoffe. Sie sind kettenförmig und in den Molekülen nur über Einfachbindungen verbunden. Als einfachstes Alkan zählt das Methan (CH4). Dieses besteht aus einem Kohlenstoffatom, welches je ein Elektronenpaar mit vier Wasserstoffatomen ausbildet. Diese vier bindenden Elektronenpaare stoßen sich gegenseitig ab und nehmen den größtmöglichen Abstand zueinander ein, weshalb die vier Wasserstoffatome ein Tetraeder bilden, in dessen Zentrum sich das Kohlenstoffatom befindet. Methan zählt als Hauptbestandteil des Erdgases und zählt als ein starkes Treibhausgas, welches einen viermal höheren Treibhauseffekt aufweist als Kohlenstoffdioxid.
| Name | verkürzte Strukturformel | Summenformel |
|---|---|---|
| Methan | CH4 | CH4 |
| Ethan | CH3-CH3 | C2H6 |
| Propan | CH3-CH2-CH3 | C3H8 |
| Butan | CH3-(CH2)2-CH3 | C4H10 |
| Pentan | CH3-(CH2)3-CH3 | C5H12 |
| Hexan | CH3-(CH2)4-CH3 | C6H14 |
| Heptan | CH3-(CH2)5-CH3 | C7H16 |
| Octan | CH3-(CH2)6-CH3 | C8H18 |
| Nonan | CH3-(CH2)7-CH3 | C9H20 |
| Decan | CH3-(CH2)8-CH3 | C10H22 |
Es sind zahlreiche Kohlenwasserstoffe mit einer Methan ähnlichen Struktur bekannt, welche in der homologen Reihe der Alkane zusammengefasst werden. Hierbei beschreibt der Wortstamm die Anzahl der Kohlenstoffatome in einem Alkanmolekül. Die Namen der Alkane werden aus diesen Wortstämmen und der Endung -an gebildet.
Die Alkane unterscheiden sich immer um eine Kohlenstoffatom und zwei Wasserstoffatome, also um eine -CH2-Gruppe. Daraus lässt sich die allgemeine Summenformel für die Alkane ableiten: CnH2n+2
Aufgrund der immer gleichen Sturktur der Alkane zeigen sie ähnliche chemische und physikalische Eigenschaften. Ein Beispiel hierfür ist die Verbrennung: Alkane verbrennen bei ausreichender Sauerstoffzufuhr immer vollständig unter Wärmeabgabe zu Kohlenstoffdioxid und Wasser.